知名Nature子刊發布騰訊AI+醫療聯合研究
騰訊AI Lab在AI+醫療應用上再進一步,世界知名期刊Nature旗下的子刊Nature Communications發布了一篇由騰訊AI Lab、美國聖路易斯華盛頓大學(WUSTL)Jianmin Cui Lab和加拿大不列顛哥倫比亞大學(UBC)David Fedida Lab的合作研究成果,解開了多年來KCNQ1通道失活機制的難題。KCNQ1是與心臟疾病密切相關的、由一種重要鉀離子通道控制的心率調節機制,該研究為心率異常診斷與治療的進一步臨床研究提供了新的思路。

鏈接:https://www.nature.com/articles/s41467-017-01911-8
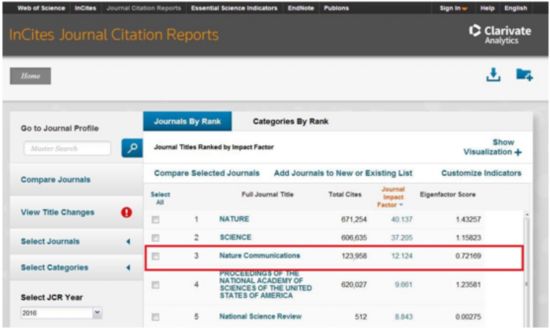
該最新研究成果發表於世界知名期刊Nature旗下的子刊Nature Communications上,該期刊影響因子12.124,在JCR綜合科學(Multidisciplinary Science)分區統計的所有SCI索引期刊中排名第三,僅次於知名的Nature與Science。
在心臟中,KCNQ1鉀離子通道控制著動作電位的復極化,其上的點突變經常會導致心臟病發生。KCNQ1通道有特殊的開關機制,並且表現出不同於其他離子通道的失活特性,對該失活特性的闡明對通道的工作機制、心臟病的病理及治療至關重要。本文結合熒光電生理、單通道記錄以及數據驅動馬爾科夫過程建模的方法揭示了KCNQ1通道的失活機制。
美國聖路易斯華盛頓大學的Jianmin Cui Lab多年來一直從事離子通道門控機制與藥理學研究,其科研團隊對大電導鈣激活型鉀通道(BK channel)以及KCNQ1/IKs等通道的研究始終引領潮流且在國際上享有廣泛聲譽。而加拿大不列顛哥倫比亞大學(UBC)David Fedida LabDavid Fedida Lab此前對IKs的單通道特性有深入研究,這是首次成功對KCNQ1的單通道進行直接實驗記錄。兩個研究室的成果均多次在國際頂級期刊發表。
騰訊AI Lab搶灘布局AI+醫療
AI+醫療產業增勢矚目,可能成為AI技術落地的第一隻靴子。作為騰訊企業級人工智能實驗室,騰訊AI Lab利用基礎研究+應用探索結合的雙重優勢,搶灘布局醫療行業。
2017年8月,由騰訊互聯網+合作事業部牽頭發布公司首款AI醫療產品「騰訊覓影」時,AI Lab支持的食管癌早期篩查是首個進入臨床預試驗項目,篩查一個內鏡檢查用時不到4秒,發現准確率高達90%。
2017年11月,「騰訊覓影」將AI+醫療技術從影像擴展到輔助診斷,由AI Lab提供獨家技術支持,將自然語言處理、機器學習與海量醫療數據結合,輔助醫生更准確理解病案,降低風險及提升診斷水准。
當月,國家科技部公布的新一代工人智能發展規劃中,騰訊有幸首批入選(全國共四家),並主導建設醫療影像國家人工智能開放創新平台。
研究背景
美國心臟病協會(American Heart Association)有七項心臟健康指標(cardiovascular health metrics)來衡量成年人的心血管健康程度,分為四項心臟健康行為指標(cardiovascular health behaviors)與四項心臟健康因素指標(cardiovascular health factors)[2]。最近的一份美國心臟病學會雜志(Journal of the American college of cardiology)上關於中國成人的心血管健康狀況的調查報告表明,在中國,滿足所有四個四項心臟健康因素指標人有13.5%,滿足所有四個四項心臟健康行為指標的人僅有7‰,而七項健康指標全部滿足的人更為跌至2‰[3]。女性通常隻滿足這七項指標中的四至五項,而男性更是僅有三至四項指標達到理想狀態[3]。在如此嚴峻的現狀下,對心臟病的深入研究刻不容緩。
心率是衡量正常人安靜狀態下每分鐘心跳次數的一種指標,該指標與心臟疾病密切相關。最重要的心率調節機制之一由一種重要的鉀離子通道控制,即KCNQ1通道。在心臟中,KCNQ1通道與其輔助亞基KCNE1結合形成IKs通道,來實現鉀離子的泵出而使心臟動作電位復極化,因此該通道是決定心率快慢最重要的因子之一。
KCNQ1通道約有700個氨基酸構成,近二十年來,臨床研究已經發現該通道上有超過300個點突變可以導致心臟病,而其中有相當一部分突變會影響通道的失活特性,因此對KCNQ1通道的失活機制的研究顯得格外重要。
常見的通道失活有N型失活(Nterminal,相對較快)和C型失活(Cterminal,相對較慢),而在KCNQ1鉀離子通道中存在一種特有的失活,它沒有典型的N型或C型失活特性,且隻有在特定的電壓刺激下才會出現(如下圖1所示)。因此其發生機制一直難以捉摸。
圖1在特定電壓刺激下,KCNQ1通道表現出“失活”特性,如圖中hook(鉤)電流所示。
此前,聖路易斯華盛頓大學Cui Lab曾於2014年發現KCNQ1通道特有的門控機制[4]。不同於其它離子通道隻有一個開放態,該通道有兩個不同的開放態: 中間開放態(intermediate open state, IO)和全開放狀態(activated open state, AO)。
本文中,研究人員發現AO開放態實際就是KCNQ1通道所謂的“失活態”。因為通道的失活特性與其AO開放態有相同的時間依賴以及電壓依賴(如下圖2a所示),並且位於通道第六個跨膜結構上的兩個點突變S338F和F351A可以分別選擇性的隻在IO和AO態開放,而因為它們都隻有一個開放態,所以這兩個突變體通道都不再具有失活特性(如下圖2b,c所示)。研究人員還從單通道電流水平上找到了KCNQ1通道“失活”的依據:AO態比IO態的開放機率低(如下圖2d所示)。這也是首次對KCNQ1單通道電流的直接記錄,實驗顯示它的電通道電導竟然低至~0.18 pS, 這是已知的最小的單通道電導(大電導鈣激活型鉀通道的單通道電導可以大至300 pS)。
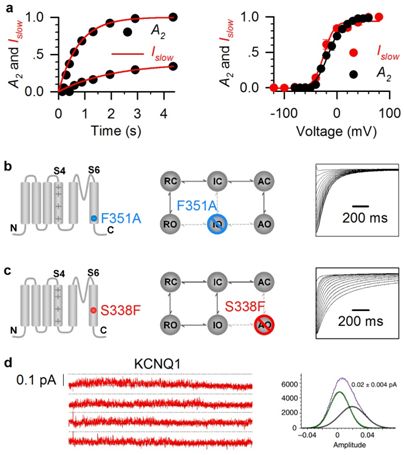
圖2 (a) KCNQ1通道的失活特性(A2)與其AO開放態(Islow)具有相同的時間依賴以及電壓依賴特性。(b-c)S338F和F351A可以分別選擇性的隻在IO和AO態開放,因此都不再具有失活特性。 (d) KCNQ1通道的單通道電流。
接著,研究人員還通過數據驅動的方法進一步研究了KCNQ1通道的“失活”特性。具體地,文章中建立了一種包括IO態與AO態在內的六態馬爾科夫模型(Six-State Markov Model)。在該六態模型中,研究人員假設其一步轉移概率與時間無關,即齊次馬爾科夫模型。此后,該研究對該齊次馬爾科夫模型的一步轉移概率矩陣進行建模,並擬合出最優參數(如下圖3a所示)。在該一步轉移概率矩陣的參數中,KRI, KIR, KIA, KAI均為電壓的函數,這使得研究人員可以對不同電壓下的KCNQ1通道的“失活”特性建立不同的齊次馬爾科夫模型。最后,該研究通過科爾莫哥洛夫向前與向后方程
(Kolmogorov Forward/Backward Equation)以及馬爾科夫過程平穩分布的性質,成功地仿真出了KCNQ1通道在不同電壓下的動態與穩態輸出,即不同的“失活”特性(如下圖3b所示)。至此,該研究在更深刻理解KCNQ1通道“失活”特性的同時,進一步証明了論文中所提出模型的正確性。
圖3 KCNQ1 通道的模型建立以及對其“失活”特性的仿真。
該文章推進了KCNQ1通道門控機制以及相關病理的研究。近年來,隨著結構生物學的高速發展,越來越多的離子通道結構被解析,但是對離子通道如何開關的研究依然是領域內的熱點及難點。該研究表明KCNQ1通道的AO態可能有著不同於經典的電壓感受區與孔區的耦合機制,為非經典的耦合機制(non-canonical VSD-pore coupling mechanism)的研究找到了突破口。
該研究為騰訊AI Lab與國際知名大學美國聖路易斯華盛頓大學,及加拿大不列顛哥倫比亞大學在AI+醫療領域的最新成果。該研究為心率異常診斷與治療的進一步臨床研究提供了新的思路。
未來,騰訊AI Lab將繼續在AI+醫療戰略的指導下,與國際知名大學/醫學院深入合作,用AI技術攻克一系列醫學挑戰。
[1] Panpan Hou, Jodene Eldstrom, Jingyi Shi, Ling Zhong, Kelli McFarland, Yuan Gao, David Fedida, Jianmin Cui. Inactivation of KCNQ1 potassium channels reveals dynamic coupling between voltage sensing and pore opening. Nature Communications 8(1):1730, 2017.
[2] 美國心臟病協會為American Heart Association。七項心臟健康指標(Cardiovascular Health Metrics)分別為:是否吸煙,體重指數,體育鍛煉,飲食健康,血脂,血壓,以及血糖。四項心臟健康行為指標(Cardiovascular Hhealth Behaviors)包括是否吸煙,體重指數,體育鍛煉,飲食健康。四項心臟健康因素指標(Cardiovascular Health Factors)包括是否吸煙,血脂,血壓,血糖。是否吸煙既為心臟健康行為指標,又被算作心臟健康因素指標。
[3] Yufang Bi, Yong Jiang, Jiang He, Yu Xu, Limin Wang, Min Xu, Mei Zhang, Yichong Li, Tiange Wang, Meng Dai, Jieli Lu, Mian Li, Chung-Shiuan Chen, Shenghan Lai, Weiqing Wang, Linhong Wang, Guang Ning. Status of Cardiovascular Health in Chinese Adults. Journal of the American College of Cardiology, 65(10): 1013-1025, 2015.
[4] Mark Zaydman, Marina Kasimova, Kelli McFarland, Zachary Beller, Panpan Hou, Holly E Kinser, Hongwu Liang, Guohui Zhang, Jingyi Shi, Mounir Tarek, Jianmin Cui. Domain–domain interactions determine the gating, permeation, pharmacology, and subunit modulation of the IKs ion channel. eLife, 3:e03606, 2014.
分享讓更多人看到 
相關新聞
- 評論
- 關注





















 第一時間為您推送權威資訊
第一時間為您推送權威資訊
 報道全球 傳播中國
報道全球 傳播中國
 關注人民網,傳播正能量
關注人民網,傳播正能量